CRISPR er et begreb inden for DNA-forskning. Det står for clustered regularly-interspaced short palindromic repeats. Disse sekvenser indgår i den genetiske kode i prokaryoter: de fleste bakterier og arkæer har dem. CRISPR-systemet fungerer som deres forsvar mod angreb fra vira og blev først karakteriseret i det 21. århundrede.
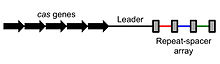
CRISPR består af korte gentagne sekvenser (repeats) adskilt af unikke sekvenser (spacers). Spacers er stumper af DNA fra tidligere virusangreb og fungerer som et genetisk "hukommelsesarkiv" — et adaptivt immunsystem, der lader prokaryoter genkende og neutralisere kendte trusler som bakteriofager. Når samme virus forsøger at inficere cellen igen, bruges disse spacer-sekvenser som vejledning til at finde og skære virus-DNA.
Hvordan CRISPR/Cas virker
Tre trin beskriver typisk CRISPR-funktionen:
- Adaptation (erhvervelse): Når en bakterie møder et nyt virus, kan en kopi af et lille stykke af virusets DNA blive indsat som en spacer i CRISPR-arrayet.
- Expression (udtryk): CRISPR-arrayet transskriberes til et langt præ-crRNA, som herefter bliver kløvet til korte crRNA-molekyler, hver indeholdende en spacer-sekvens, der svarer til tidligere angreb. Mange systemer kræver også et tracrRNA, som hjælper med at modne crRNA og danne en kompleks med Cas-proteinet.
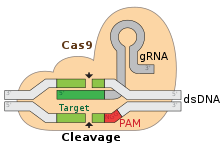
- Interference (angreb): crRNA guider et Cas-enzym (fx Cas9) til det matchende virus-DNA; Cas-enzymet skærer målet, så viruset ikke kan reproducere sig.
For at Cas-enzymet kan genkende korrekt mål kræves ofte et kort nabomotiv ved målet, kaldet PAM (protospacer adjacent motif). PAM sikrer, at bakterien ikke skærer i sit eget CRISPR-array.
Typer af CRISPR/Cas-systemer
Der findes flere typer CRISPR-systemer (type I, II, III m.fl.). I praksis er Cas9 (fra Streptococcus pyogenes) et af de mest anvendte værktøjer til laboratorie-redigering. Andre vigtige enzymer er Cas12 (DNA-skæring med lidt andre egenskaber) og Cas13, som målretter RNA i stedet for DNA og derfor har anvendelser inden for RNA-redigering og diagnostik.
Anvendelser
- Genredigering: CRISPR bruges til at skære og indsætte eller ændre gener i celler, hvilket har revolutioneret genetik og molekylærbiologi. Det er et præcist, effektivt og relativt billigt værktøj sammenlignet med tidligere metoder.
- Genterapi: Forskere arbejder på at bruge CRISPR til at behandle arvelige sygdomme ved at rette mutationer i menneskelige celler. Der er kliniske forsøg i gang, især med ex vivo-redigering af blodstamceller til sygdomme som sigdcelleanæmi og beta-thalassæmi.
- Bioteknologi og landbrug: Udvikling af planter og dyr med forbedrede egenskaber (fx sygdomsresistens eller bedre ernæringsindhold) ved hjælp af genetisk modificering.
- Diagnostik: Systemer med Cas12/Cas13 udnyttes i følsomme tests for virus og andre patogener (fx metoder som SHERLOCK/DETECTR), hvor tilstedeværelsen af målsekvensen giver et målbart signal.
- Forskning i genfunktion: Hurtig fremstilling af knockout- eller modificerede organismer til grundforskning.
Udviklinger inden for redigeringsteknikker
Ud over klassisk "skær og indsæt" er der kommet nye varianter som base editing (ændrer enkelte DNA-baser uden at lave dobbeltstrenget brud) og prime editing (kan indsætte, slette eller erstatte korte DNA-sekvenser med færre biprodukter og potentielt færre off-target-effekter). Disse metoder udvider mulighederne og forbedrer præcisionen.
Levering, begrænsninger og sikkerhed
En af de største praktiske udfordringer er, hvordan man leverer CRISPR-systemet ind i de relevante celler i en organisme. Metoder omfatter virale vektorer (fx AAV), lipid-nanopartikler, elektroporation og ex vivo-redigering af celler, som efterfølgende sættes tilbage.
Der er også tekniske begrænsninger såsom off-target-effekter (utilsigtede ændringer andre steder i genomet), mosaik i udviklende væv og immunreaktioner mod Cas-proteiner. Nøjagtig målretning, forbedrede Cas-varianter og streng validering af ændringer er aktive forskningsområder.
Etik og regulering
CRISPR rejser vigtige etiske spørgsmål, især i forbindelse med rettelser i kimlinjen (ændringer, der kan nedarves). Etablerede tilfælde som uautoriseret ændring af menneskelige embryoer har ført til stærk kritik og øget regulering. Mange lande har derfor klare regler, og et globalt etisk og juridisk rammeværk diskuteres fortsat.
Historie og perspektiver
Selvom CRISPR som fænomen blev observeret tidligere, blev den molekylære mekanisme og potentialet for genredigering tydeligt i begyndelsen af 2010'erne. I 2020 fik Jennifer Doudna og Emmanuelle Charpentier Nobelprisen i kemi for udviklingen af CRISPR/Cas9 som et genome‑redigeringsværktøj. Siden da har feltet udviklet sig hurtigt med mange kliniske forsøg og nye teknologier.
Opsummering: CRISPR er både et naturligt immunforsvar hos mange prokaryoter og et kraftfuldt forskningsværktøj, der muliggør målrettet ændring af DNA og RNA. Det åbner store muligheder inden for medicin, landbrug og bioteknologi, men stiller også krav om omhyggelig vurdering af sikkerhed, etik og regulering.