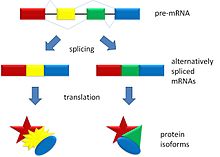
Alternativ splejsning gør det muligt for DNA at kode for mere end ét protein ved at variere sammensætningen af exonerne i det modne messenger-RNA'et. Fra ét enkelt gen kan der fremkomme flere forskellige mRNA-isoformer, som oversættes til proteiner med forskellig størrelse, funktion eller lokalisation. Dermed øger alternativ splejsning den funktionelle kompleksitet af et genom uden at der kræves flere gener.
Hvordan virker splejsning?
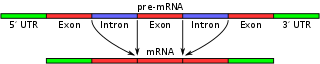
Under transkription dannes først et forstadium kaldet pre-mRNA, som indeholder både exonerne (kodende sekvenser) og introns (ikke-kodende sekvenser). Ved RNA-splejsning fjernes introns, og exonerne sættes sammen til et modent mRNA. Denne proces styres af splejso-somet (splejsosomet) — et stort enzymkompleks bestående af små nukleare ribonukleoproteiner (snRNP'er, f.eks. U1, U2, U4/U6•U5) og mange associerede proteiner — samt af cis-regulatoriske elementer på RNA'et såsom 5'- og 3'-splejsesites, forgreningsstedet og polypyrimidin-træk. Derudover påvirker trans-virale faktorer som splicing-aktivatorer og -repressorer hvilke sites der benyttes.
Typer af alternativ splejsning
Der findes flere former for alternativ splejsning, blandt de mest almindelige er:
- Exon-skipping — et helt exon inkluderes i nogle isoformer og udelades i andre.
- Alternativt 5'- eller 3'-splejsesite — ændret start- eller slutpunkt for et exon, hvilket kan forskyde læserammen.
- Mutually exclusive exons — kun ét af to (eller flere) alternative exoner indgår i hver isoform.
- Intron retention — et intron bevares i det modne mRNA, ofte med funktionelle konsekvenser.
Disse mekanismer er reguleret vævs- og udviklingsspecifikt, så et gen kan give forskellige proteiner i fx muskel, hjerne eller lever. Der opstår løbende nye varianter af alternativ splejsning, og forskningen afdækker stadig flere nuancer.
Betydning for proteiner og sygdom
Alternativ splejsning kan ændre proteiners domæner, stabilitet, subcellulær lokalisation eller interaktioner med andre molekyler. Konsekvenserne spænder fra subtile funktionelle forskelle til fuldstændigt tab af funktion eller opståen af skadelige egenskaber (gain-of-function eller dominant-negativ effekt).
Unormale variationer i splejsning er forbundet med mange sygdomme. Mange genetiske sygdomme skyldes mutationer, der påvirker normale splejsesites eller regulatoriske elementer og dermed fører til forkert splejsning. Desuden bidrager fejl i splejsningskontrollen til kræft, hvor mutationer i splicing-faktorer (fx SF3B1, SRSF2, U2AF1) kan ændre splejsningen globalt og fremme tumorudvikling.
Ikke-fungerende eller forkert splejsede mRNA'er genkendes ofte af cellens kvalitetskontrol og nedbrydes via mekanismer som nonsense-medieret mRNA-nedbrydning (NMD). Hvis denne kontrol svigter, kan skadelige peptider blive produceret.
Eksempler og klinisk relevans
- Spinal muskelatrofi (SMA): forskellen mellem SMN1 og SMN2 ligger i, hvordan et exon splejses ind eller udelades. Behandlinger som antisense-oligonukleotider (fx nusinersen/Spinraza) og små molekyler (fx risdiplam) ændrer splejsningen til fordel for fuldt funktionelt SMN-protein.
- Duchenne muskeldystrofi: eksklusiv udskæring af bestemte exoner i DMD-genet kan genskabe en delvis funktionel dystrofin-proteinform — dette er mål for exon-skipping-terapier (f.eks. eteplirsen for udvalgte mutationer).
- Kræft: mutationer i splicing-faktorer eller regulatoriske sekvenser kan skabe onkogene isoformer eller fjerne tumor-suppressor funktioner.
Hvordan opdages og undersøges alternativ splejsning?
Moderne metoder gør det muligt at kortlægge splejsningsmønstre detaljeret:
- RNA-sekventering (RNA-seq) med «splice-aware» aligners giver kvantificering af isoformer og opdager nye splejsningsarrangementer.
- RT-PCR og qPCR bruges til målrettet analyse af specifikke splejsningshændelser.
- Massespektrometri kan bekræfte, at forskellige mRNA-isoformer bliver omsat til proteiner.
Terapeutiske strategier
Der udvikles flere måder at rette eller udnytte alternativ splejsning på:
- Antisense-oligonukleotider (ASO'er) — designes til at binde specifikke RNA-sekvenser og ændre splejsningsmønstret (fx fremme inklusion eller eksklusion af et exon).
- Små molekyler — kan modulere splejsosomets aktivitet eller stabilisere bestemte splice-site-interaktioner.
- Genredigering (CRISPR/Cas) — kan fjerne eller rette mutationer i splicesites eller regulatoriske elementer.
- Splice-switching therapier — klinisk anvendte tilgange for visse sygdomme som nævnt ovenfor.
Opsummering
Alternativ splejsning er en central mekanisme i eukaryoter, som øger den funktionelle kompleksitet af genomet: Hos mennesker er ~95 % af de multiexoniske gener alternativt splejset. Rigtig regulering af splejsning er nødvendig for normal fysiologi, mens fejl i splejsningen kan føre til sygdom. Forståelse af mekanismerne bag alternativ splejsning har gavnet både grundforskning og udvikling af nye behandlingsformer, og området er aktivt forsket i med henblik på diagnostik og målrettet terapi.