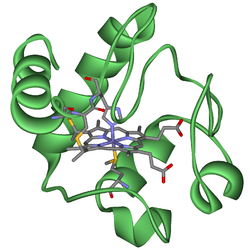
Cytochromer er hæmoproteiner (eller proteiner, der indeholder hæmgrupper). De deltager i dannelsen af ATP via elektrontransport ved at overføre elektroner mellem enzymkomplekser og dermed bidrage til opbygningen af en protongradient over membraner.
Struktur og hæmtyper
Cytochromer har en protein-del og en ikke-proteinsk prostetisk gruppe, hæm, som indeholder et jernatom. Jernet skifter reversibelt mellem oxidationsstaterne Fe2+ og Fe3+ og tillader dermed elektron-overførsel. Der findes flere typer hæm:
- Hæm b (protoporfyrin IX) — almindelig i mange membranbundne cytochromer, f.eks. i kompleks III.
- Hæm c — kovalent bundet til proteinet via thioetherbindinger til cysteinrest(er); findes i bl.a. cytochrom c.
- Hæm a — har specielle kemiske modifikationer (fx formylgruppe og en farnesylderivat) og findes i cytochromoxidase (kompleks IV).
Typer af cytochromer
- Cytochrom a og a3 — dele af cytochrom c oxidase (kompleks IV), vigtige ved ilt-reduktion.
- Cytochrom b — membranbundet, indgår i bl.a. kompleks III (cytochrom bc1-komplekset) og i fotosyntetisk b6f-kompleks.
- Cytochrom c — lille, vandopløselig, perifert bundet protein i mitokondriets mellemliggende rum; transporterer elektroner mellem kompleks III og IV.
- Cytochrom c1 — en komponent af kompleks III, der sammen med cytochrom b danner bc1-komplekset.
- Cytochrom P450 — en stor familie af hæm-thiolat monooxygenaser, vigtige i stofskifte af lægemidler og syntese/omdannelse af lipider og steroider (dog ikke altid omtalt som en klassisk del af respirationskæden).
Funktion i elektrontransportkæden
Cytochromer fungerer som elektronbærere i respirationskæden i mitokondrier, i fotosyntesens elektrontransport samt i bakterielle respirationssystemer. De overfører elektroner mellem komplekser i kæden, og nogle komplekser bruger denne elektrontransport til samtidig at pumpe protoner over en membran. Denne protongradient driver ATP-syntase og dermed produktion af ATP.
Eksempler på roller:
- Kompleks III (cytochrom bc1) overfører elektroner fra ubikinon til cytochrom c og bidrager til protonpumping via Q-cyklussen.
- Cytochrom c transporterer elektroner i opløst form mellem kompleks III og kompleks IV.
- Kompleks IV (cytochrom c oxidase) modtager elektroner fra cytochrom c og katalyserer den endelige reduktion af O2 til H2O; denne reaktion er også forbundet med protonpumping.
Biokemiske og medicinske aspekter
Udover deres centrale rolle i energimetabolisme har cytochromer flere andre betydninger:
- Apoptose: Frigivelse af mitokondrie-cytochrom c til cytosol er et vigtigt signal i den indre apoptotiske vej, hvor det aktiverer caspaser og fører til programmeret celledød.
- Farmakologi og toksikologi: Cytochrom P450-enzymer metaboliserer mange lægemidler og xenobiotika; hæmning eller induktion af disse kan ændre lægemiddelvirkning og bivirkninger.
- Sygdomme: Mutationer i cytochrom-relaterede proteiner eller i mitokondrielle gener, som påvirker elektrontransporten, kan give anledning til mitokondrie-sygdomme med nedsat energiproduktion.
- Bioteknologi: Cytochromer bruges i biosensorer og i forskning til at forstå elektrontransport og redoxkemi; P450-isoformer anvendes også i industrien til biotransformation.
Spektroskopiske egenskaber og anvendelse i forskning
Hæmgruppens konjugerede ringstruktur giver stærke absorptionsegenskaber i det synlige område, hvilket gør cytochromer lette at følge med spektroskopi. Reduktionstilstand (Fe2+ vs. Fe3+) ændrer absorptionsspektret, og mange cytochromer har et karakteristisk alfa-bånd i det røde område (f.eks. cytochrom c omkring ~550 nm i reduceret form). Sådanne egenskaber bruges til at bestemme redox-tilstand, kinetik og binding af ligander i undersøgelser.
Praktisk opsummering
- Hvad: Hæmholdige proteiner, der kan optage og afgive elektroner.
- Hvorfor: Nødvendige for effektiv elektrontransport og opbygning af den protongradient, der driver ATP-syntese.
- Hvor: I mitokondrier, kloroplaster, bakterier og i en række enzymsystemer (fx P450).
Bemærk: Cytochromers funktion og struktur er et stort forskningsområde; ovenstående er en oversigt over de vigtigste principper og eksempler.