Pentan er en organisk forbindelse med den kemiske formel C
5H
12. Det er en alkan med fem kulstofatomer. Normalt repræsenterer "pentan" alle tre isomerer (n-pentan, isopentan og neopentan). Men i IUPAC repræsenterer pentan kun n-pentan. I IUPAC er de to andre isomerer 2-methylbutan og 2,2-dimethylpropan. Cyclopentans kemiske formel er C5H10, så det er ikke en isomer af pentan.
Isomerer og IUPAC-navne
Pentan har tre strukturelle (konstitutionelle) isomerer, alle med molekylformel C5H12:
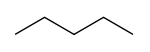
- n-Pentan (pentan) — en ukædet, lineær kæde: CH3‑CH2‑CH2‑CH2‑CH3. Ifølge IUPAC er dette forbindelsen, der officielt betegnes "pentan".
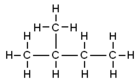
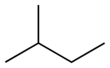
- 2‑Methylbutan (isopentan) — en forgrenet kæde: CH3‑CH(CH3)‑CH2‑CH3. Almindelig betegnelse: isopentan.
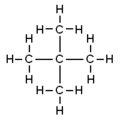
- 2,2‑Dimethylpropan (neopentan) — kraftigt forgrenet (kvartært karbon i midten): C(CH3)4. Almindelig betegnelse: neopentan.
Struktur, konformationer og egenskaber
Molekylvægten for C5H12 er cirka 72,15 g·mol−1. De tre isomerer har forskellige fysiske egenskaber pga. forskelle i forgrening og molekylær form:
- Kogepunkter (typiske værdier): n-pentan ≈ 36,1 °C, 2‑methylbutan ≈ 27,8 °C, 2,2‑dimethylpropan ≈ 9,5 °C. Forgrening sænker kogepunktet fordi molekylerne får mindre overfladekontakt og dermed lavere van der Waals‑tiltrækning.
- Tæthed: flydende pentaner har typisk tæthed omkring 0,62–0,63 g·cm−3 ved 20 °C (nærmere værdi afhænger af isomer).
- Konformation: n-pentan kan rotere omkring C–C‑bindingerne og har stabil konformation med anti‑ og gauche‑tilstande; interaktioner mellem terminale grupper (sterisk og elektronisk) påvirker energiforskelle. Neopentan er højt symmetrisk og viser mindre konformationsvarieret energi pga. det kvartære centrum.
Anvendelser og forekomst
- Pentaner anvendes som opløsningsmidler i laboratorier og industrien og indgår som komponenter i benzinfraktioner.
- De bruges også i fremstilling af siliconer, til ekstraktion og som råvarer i organisk syntese.
- Pentan findes naturligt i petroleumsråstoffer og kan forekomme i mindre mængder i naturgas.
Sikkerhed, håndtering og miljø
- Pentaner er letantændelige væsker og danner brandbare dampe; opbevares og håndteres væk fra tændkilder med god ventilation.
- Indånding af høje koncentrationer kan give hovedpine, svimmelhed eller bevidsthedstab på grund af narkotiske effekter og iltfortrængning. Langvarig eller gentagen eksponering bør undgås.
- Som flygtige organiske forbindelser (VOC) kan pentaner bidrage til ozondannelse i troposfæren. Spild håndteres som petroleumprodukt med passende opsugningsmidler og korrekt affaldshåndtering.
Bemærkninger om navngivning
Det er vigtigt at kende forskellen mellem almindelige/triviale navne og systematisk IUPAC-navngivning: i dag bruges "pentan" ofte i daglig tale om alle C5H12‑isomerer, men formelt i nomenklaturen svarer "pentan" til den lineære n‑pentan, mens de forgrenede isomerer skal navngives som 2‑methylbutan og 2,2‑dimethylpropan.