Gram-negative bakterier er bakterier, der ikke tilbageholder krystalvioletfarvestof ved Gram-farvning. Efter affarvning tilsættes en modfarve, safranin, som farver de gramnegative celler røde eller lyserøde. Farvningsforskellen skyldes strukturelle forskelle i cellevæggen: gramnegative har en tyndere peptidoglykanlag og en ydre membran, mens Gram-positive bakterier beholder krystalviolet på grund af et tykkere peptidoglykanlag.
Cellevæg og ydre membran
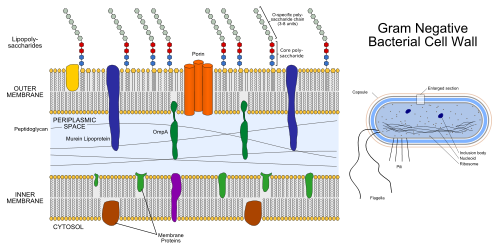
Den karakteristiske ydre membran hos gramnegative bakterier ligger yderst og fungerer som en barriere mod mange stoffer. Mellem den ydre membran og cellemembranen findes en periplasmisk rum, som indeholder et tyndt lag peptidoglykan. Ydre membranen indeholder:
- Poriner: proteinkanaler der tillader passive diffusion af små molekyler (nogle antibiotika passerer gennem poriner).
- Lipopolysaccharid (LPS): et fedt‑kulhydratkompleks der danner det yderste lag.
Lipopolysaccharid (LPS) og immunrespons
LPS består typisk af tre dele: lipid A, en kerne‑polysaccharid og et O‑antigen. Lipid A er den del, der virker endotoksisk for mennesker og andre dyr. Når immunceller genkender LPS, udløses et stærkt medfødt immunforsvar med produktion af cytokiner og aktivering af immunsystemet. Denne cytokinudskillelse kan føre til feber og lokal eller systemisk Inflammation, og ved kraftig frigivelse af LPS kan der opstå septisk chok.
Antibiotikaresistens — hvorfor gramnegative ofte er mere svære at behandle
Sammenlignet med grampositive bakterier er mange gramnegative arter mere resistente over for antibiotika, fordi den ydre membran og andre mekanismer begrænser antibiotikapassage og nedbryder eller udskiller lægemidler. Almindelige resistensmekanismer inkluderer:
- Begrænset adgang gennem poriner (nedsat permeabilitet).
- Enzymer i periplasma, fx β‑lactamaser, som inaktiverer β‑lactamantibiotika.
- Efflux‑pumper som aktivt udskiller antibiotika fra cellen.
- Mutationer i målproteiner (fx ribosomale mål eller DNA‑gyrase) der mindsker lægemidlets binding.
- Horisontal genoverførsel via plasmider og transposoner, som spreder resistensgener (fx ESBL, carbapenemaser som KPC/NDM).
Disse faktorer gør det ofte nødvendigt at bruge bredspektrede eller kombinationsbehandlinger ved alvorlige infektioner, og stigende forekomst af multiresistente gramnegative bakterier er en global sundhedsudfordring.
Klinisk og laboratoriemæssig betydning
Gramfarvning er et hurtigt diagnostisk værktøj, men identifikation og resistensbestemmelse kræver ofte dyrkning, biokemiske tests, MALDI‑TOF eller molekylære metoder (PCR). Nogle vigtige kliniske eksempler på gramnegative bakterier er Escherichia coli, Salmonella, Pseudomonas aeruginosa og Neisseria-arter — alle kan forårsage alt fra milde urinvejsinfektioner til alvorligt blodforgiftning.
Forebyggelse og behandling
Forebyggelse af spredning omfatter hygiejne, korrekt håndtering af katetre og invasive procedurer, vaccinationsprogrammer hvor relevante samt overvågning af resistensmønstre. Behandling vælges ud fra lokale resistensdata og ofte efter resistensbestemmelse; mulige antibiotikagrupper mod gramnegative infektioner omfatter aminoglykosider, fluoroquinoloner, cephalosporiner og carbapenemer, men valg er afhængigt af art og resistensprofil.
Forståelsen af gramnegative bakteriers struktur, LPS‑virkning og resistente mekanismer er central for både klinisk behandling og infektionskontrol.