Glykogen (almindeligvis kendt som animalsk stivelse, selv om dette navn er unøjagtigt) er et polysaccharid, som er den vigtigste form for glukoseopbevaring i dyreceller.
Glykogen findes i form af granulater i cytosolen i mange celletyper og spiller en vigtig rolle i glukosecyklussen. Glykogen udgør en energireserve, der hurtigt kan mobiliseres for at opfylde et pludseligt behov for glukose, men som er mindre kompakt end energireserverne i form af triglycerider. Kun det glykogen, der er lagret i leveren, kan gøres tilgængeligt for andre organer.
Struktur og opbygning
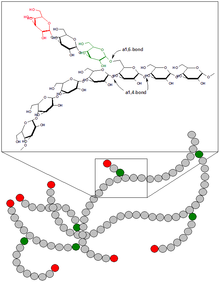
Glykogen er et forgrenet polymer af glukoseenheder bundet hovedsageligt ved alpha-1,4-glykosidbindinger med forgreningspunkter dannet af alpha-1,6-glykosidbindinger. Molekylet har en proteinkerne kaldet glykogenin, som fungerer som primer for syntesen. De organiske enheder danner granulater, som kan eksistere som mindre beta-partikler (enkeltmolekyler) eller større alfa-klynger (sammenklumpede partikler).
Syntese og nedbrydning
Glykogensyntese (glycogenese) og glykogennedbrydning (glykogenolyse) styres af specifikke enzymer:
- Syntese: Glycogen synthase tilføjer glukoseenheder fra UDP-glukose til de voksende kæder, mens branching enzyme (amylo-(1,4→1,6)-transglycosylase) danner forgreningerne.
- Nedbrydning: Glycogen phosphorylase kløver alpha-1,4-bindinger og frigiver glukose-1-fosfat. Et debranching-enzym håndterer alpha-1,6-forgreningerne, så komplette glukoseenheder kan frigives.
Forskellen i enzymatisk udstyr betyder også, at leverceller kan omdanne glykogen til frit glukose via glucose-6-phosphatase, mens muskelceller normalt mangle denne evne og bruger den frigivne glukose-1-fosfat til egen energiproduktion.
Regulering
Glykogenmetabolismen er nøje reguleret for at bevare blodsukkeret og tilpasse energitilførslen ved aktivitet:
- Insulin fremmer glykogensyntese ved at aktivere proteinfosfataseer, som defosforylerer og aktiverer glycogen synthase.
- Glucagon (i leveren) og adrenalin/epinephrin (især i leveren og muskler) stimulerer glykogennedbrydning via cAMP/PKA-kaskaden, der aktiverer glycogen phosphorylase.
- Muskelaktivitet øger brugen af glykogen gennem stigninger i AMP og calcium, som aktiverer phosphorylase-kinase uafhængigt af hormoner.
Fysiologiske roller
- Lever: Leverglykogen fungerer som buffer for blodglukoseniveauet mellem måltider og under faste.
- Muskler: Muskler lagrer glykogen til hurtig energi ved kontraktioner under aktivitet — dette glykogen bruges primært lokalt og kommer ikke i betydelig grad ind i blodbanen.
- Andre væv: Hjernen og visse andre celler har lille eller ingen glykogenlagring, men astrocytter i hjernen indeholder noget glykogen, som kan støtte neurale funktioner under stress.
Mængder og effektivitet
Hos et voksent menneske indeholder lever og skeletmuskulatur størstedelen af kroppens glykogen; mængder varierer med kost, træningsstatus og kropstype. Glykogen binder vand (omtrent 2–3 g vand pr. g glykogen), hvilket gør det mindre kompakt end fedt (triglycerider), som lagres uden at binde så meget vand.
Klinisk betydning
- Glykogenlagringssygdomme: Arvelige defekter i enzymerne, der håndterer glykogen, fører til en gruppe sygdomme kaldet glykogenlagringssygdomme (f.eks. von Gierke sygdom type I — glucose-6-phosphatase-mangel; McArdle sygdom type V — muskelfosforylase-mangel). Symptomer kan omfatte hypoglykæmi, muskeltræthed, vækstproblemer og forstørret lever afhængigt af typen.
- Diagnostik: Væv kan farves for glykogen med Periodic acid–Schiff (PAS) reaktion, og enzymniveauer eller genetiske tests kan bekræfte specifikke defekter. Blodsukker- og laktatmålinger ved træning kan også vejlede ved muskelsygdomme.
Opsummering
Glykogen er en hurtig og regulerbar energireserve i dyr, vigtig for at opretholde blodsukker og levere brændstof til aktive muskler. Dens hurtige mobilisering gør den afgørende i kortvarige, højintensitetsbehov, mens triglycerider fungerer som kroppens langsigtede, mere kompakte energilager.