Kromofor er den del af et molekyle, der absorberer lys og dermed bestemmer stoffets synlige farve. Når et molekyle optager bestemte bølgelængder af synligt lys, bliver disse bølgelængder ikke reflekteret eller transmitteret — kun de øvrige bølgelængder når vores øjne, hvilket giver det indtryk af en bestemt farve.
Hvordan virker en kromofor?
Farven kommer typisk fra elektroniske overgange i kromoforen. I mange organiske kromoforer er der et system af konjugerede dobbeltbindinger eller aromatiske ringe, hvor pi-elektroner kan bevæge sig over et større område. Når et foton rammer molekylet, kan et af disse elektroner excitere fra et lavere energiniveau (ofte π) til et højere (ofte π*). Energien af den absorberede foton svarer til forskellen mellem disse niveauer — og den ligger for synligt lys i bestemte intervaller, afhængigt af kromoforens struktur.
Vigtige begreber
- Konjugation: Længere konjugerede systemer sænker energiforskellen mellem niveauer og fører typisk til absorption ved længere bølgelængder (rødere farver).
- Elektroniske overgangstyper: Almindelige overgange er π→π* og n→π* (hvor n er ikke-bindende elektroner, fx på oxygen eller nitrogen).
- Auxokrome grupper: Visse sidegrupper (fx –OH, –NH2) ændrer absorptionens intensitet og position ved at donere eller trække elektroner, hvilket kan give skift i farven.
- Bathokromisk / hypsochromisk: Bathokromisk (rødforskydning) betyder absorption ved længere bølgelængder; hypsochromisk (blåforskydning) betyder absorption ved kortere bølgelængder.
- Hyperkromisk / hypokromisk: Ændringer i absorptionsintensitet (større eller mindre absorption ved en given bølgelængde).
Typer og konkrete eksempler
Der findes mange naturlige og syntetiske kromoforer. Nogle velkendte eksempler:
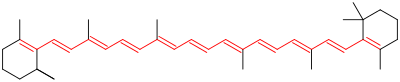
- β-caroten — konjugeret polyen, giver orange farve i gulerødder og mange frugter.
- Chlorofyl — grøn plantepigment, vigtigt for fotosyntese; har en porfyrinring med et udstrakt konjugeret system.
- Hæmoglobin / heme — jernholdig porfyrin, ansvarlig for blodets røde farve.
- Retinal — kromofor i øjets fotoreceptorer, ændrer konfiguration ved lysindfald og starter synsprocessen.
- Azo-grupper (–N=N–) — almindelige i farvestoffer og indigo/azo-dyes med skarpe farver.
Måling og anvendelse
Kromoforer karakteriseres ofte ved UV-Vis spektroskopi: et spektrum viser, hvilke bølgelængder der absorberes og med hvilken intensitet (molar absorptivitet). Disse målinger bruges til at identificere forbindelser, bestemme koncentrationer og studere reaktioner, hvor kromoforer ændrer struktur.
Biologisk betydning
I biologiske molekyler, der fanger eller registrerer lysenergi, er kromoforen den del af molekylet, der reagerer, når det rammes af lys. Kromoforer indgår i processer som fotosyntese, syn og kemiske signaleringsveje. Kromoforer er også ræsonnerende komponenter i mange kromatoforer, som er de pigmentholdige og lysreflekterende celler, der findes i mange dyr og bruges til farve, kamuflage og kommunikation.
Faktorer der påvirker farven
- Strukturændringer: Ændring i kædelængde eller konjugation påvirker absorptionens bølgelængde.
- Substituenter: Elektrondonerende eller -tiltrækkende grupper kan forskyde og ændre absorptionsintensiteten.
- Miljø: Opløsningsmiddel, pH og binding til proteiner kan ændre kromoforens spektrale egenskaber (solvatochromisme, pH-følsomhed).
- Kompleksering: Metalioner bundet til en kromofor (fx i porfyriner) kan give nye absorptionsbånd eller ændre farven.
Praktiske anvendelser
Kromoforer anvendes i farvestoffer, indikatorer (pH-indikatorer), sensorer, fluorescent mærkning (hvor kromoforen eller en beslægtet fluorofor udsender lys) og optiske materialer. I medicin og bioteknologi bruges kromoforer til at mærke molekyler, så man kan følge biologiske processer med spektroskopi eller billeddannelse.
Kort sagt er en kromofor den struktur i et molekyle, som bestemmer hvilke bølgelængder af synligt lys der absorberes — og derfor hvilken farve et stof fremtræder med. Forståelse af kromoforens kemi gør det muligt at designe farver, sensorer og lysfølsomme molekyler med ønskede egenskaber.