En kemisk celle omdanner kemisk energi til elektrisk energi. De fleste batterier er kemiske celler. En kemisk reaktion finder sted i batteriet og får elektrisk strøm til at strømme. Enkelt sagt omdannes energi fra stoffer inde i cellen til elektroner, som bevæger sig gennem en ydre leder og kan udføre arbejde (fx drive en lampe eller en motor).
Hvordan virker en kemisk celle?
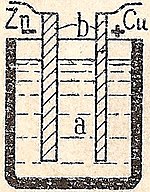
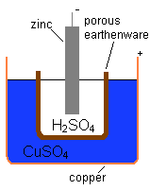
En kemisk celle består typisk af tre hoveddele:
- Anoden (negativ elektrode under afladning) hvor oxidation finder sted (stoffer afgiver elektroner).
- Kathoden (positiv elektrode under afladning) hvor reduktion finder sted (stoffer optager elektroner).
- Elektrolytten, en ionledende substans som forbinder de to elektroder internt og gør det muligt for ioner at bevæge sig for at opretholde elektronneutralitet.
Når cellen aflades, bevæger elektronerne sig fra anoden gennem den ydre kreds til kathoden. I selve cellen sker der en redoxreaktion (reduktion-oxidation), som er selve kilden til den elektriske spænding. En enkelt kemisk celle har et bestemt spændingsniveau, mens et "batteri" ofte består af flere celler for at opnå højere spænding eller kapacitet.
Typer af batterier (kort oversigt)
Man deler ofte batterier i to hovedkategorier:
- Primære batterier (ikke-genopladelige) — producerer elektricitet indtil de kemiske stoffer er opbrugte. Eksempler: alkaline-batterier, zink-kul (zink-carbon), nogle lithium-primære celler. De er praktiske til engangsbrug og udskiftes, når de er tomme.
- Sekundære batterier (genopladelige) — kan genoplades ved at føre strøm tilbage gennem cellen og derved gendanne de oprindelige kemikalier. Almindelige typer: bly-syre (bruges i biler), NiCd (nikkel-cadmium), NiMH (nikkel-metalhydrid) og moderne lithium-ion (bruges i smartphones, elbiler og bærbare computere).
Der findes også specielle typer som flow-batterier (bruges i store energilagringsanlæg), brændselsceller (omdanner brændstof kemisk til elektricitet kontinuerligt, fx brintceller) og nye teknologier som faste-state-batterier under udvikling.
Vigtige tekniske begreber
- Spænding (V) — den elektriske potentialforskel en celle leverer; bestemt af de anvendte kemikalier.
- Kapacitet (mAh eller Ah) — hvor meget elektrisk ladning batteriet kan levere over tid; angiver hvor længe en enhed kan køre ved en given strømstyrke.
- Energitæthed (Wh/kg) — hvor meget energi batteriet kan lagre i forhold til vægt; vigtig for bærbare enheder og køretøjer.
- Power density — hvor hurtigt energi kan leveres (vigtig for startmotorer og høj-effekt-anvendelser).
- Indre modstand og selvafladning — påvirker hvor effektivt og hvor længe en celle kan levere strøm uden tab.
- Cykelliv — antal fulde opladnings-/afladningscyklusser et genopladeligt batteri kan tåle før kapaciteten falder betydeligt.
Anvendelser og eksempler
Batterier findes i mange størrelser og til mange formål: fra små knapcellebatterier i ure og medicinsk udstyr, AA- og AAA-batterier i fjernbetjeninger og legetøj, batterier i kameraer, til store batteripakker i biler, busser, og industrielle energilager. Endnu større batterisystemer bruges i energiopbevaring til elnettet — og ubåde kræver meget store batterier til at operere under vand.
Sikkerhed, miljø og bortskaffelse
Batterier kan indeholde giftige eller brandfarlige materialer. Forkert behandling kan føre til lækage, brand eller eksplosion (fx termisk runaway i nogle litium-batterier). Derfor er der anbefalinger for sikker opladning, opbevaring og transport. Genbrug og korrekt bortskaffelse er vigtige for at reducere miljøpåvirkning og genvinde værdifulde materialer som kobolt, lithium, bly og nikkel. Mange steder findes indsamlingssystemer og genbrugsordninger for batterier.
En kort historisk note
De første genopladelige batterier blev udviklet af den franske ingeniør Gaston Planté i 1859 (bly-syre-batteriet). Siden da er teknologien udviklet kraftigt med nye materialer og design, som har øget både energitæthed, levetid og sikkerhed.
Samlet set er en kemisk celle en praktisk måde at lagre og frigive energi på gennem kontrollerede kemiske reaktioner. Valg af type batteri afhænger af anvendelse, krav til vægt, pris, sikkerhed og miljøhensyn.