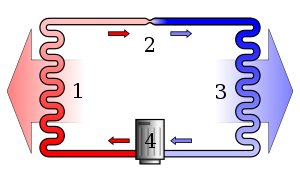
Termodynamikkens anden lov siger, at når energi skifter fra en form til en anden form, eller når stof bevæger sig frit, øges entropien (uorden) i et lukket system.
Forskelle i temperatur, tryk og massefylde har en tendens til at udjævne sig horisontalt efter et stykke tid. På grund af tyngdekraften udjævnes massefylde og tryk ikke vertikalt. Tætheden og trykket vil være større i bunden end i toppen.
Entropi er et mål for spredningen af stof og energi til alle de steder, hvor de har adgang.
Den mest almindelige formulering af termodynamikkens anden lov skyldes i det væsentlige Rudolf Clausius:
Med andre ord forsøger alting at opretholde den samme temperatur over tid.
Der findes mange forskellige udtryk for den anden lov, som alle har samme betydning, men som alle bruger forskellige udtryk. Et andet udsagn af Clausius er:
Varme kan ikke i sig selv passere fra et koldere til et varmere legeme.
En tilsvarende udtalelse fra Lord Kelvin er:
En omdannelse, hvis eneste slutresultat er at omdanne varme, der udvindes fra en kilde med konstant temperatur, til arbejde, er umulig.
Den anden lov gælder kun for store systemer. Den anden lov handler om den sandsynlige adfærd i et system, hvor der ikke kommer energi eller stof ind eller ud. Jo større systemet er, jo mere sandsynligt er det, at den anden lov vil være sand.
Hvad menes med entropi?
Entropi måler, hvor mange måder et system kan arrangeres på, uden at de makroskopiske størrelser (tryk, volumen, temperatur) ændrer sig. I den statistiske fortolkning giver Boltzmanns formel sammenhæng mellem entropi og antallet af tilgængelige mikrotilstande W:
S = k·ln W, hvor k er Boltzmanns konstant (≈ 1,38·10⁻²³ J/K). Entropi måles i enheden J/K.
På et intuitivt plan kan man tænke på entropi som et mål for spredning: varmeenergi, partikler eller information, der bliver fordelt over flere tilstande eller steder, øger entropien.
Matematisk og praktisk anvendelse
I termodynamikken skrives ændringen i entropi for en reversibel varmeoverførsel som
dS = δQ_rev / T,
hvor δQ_rev er den reversible varme, og T er den absolutte temperatur. For irreversible processer er den samlede entropi i et isoleret system stigende eller konstant; den kan aldrig falde:
ΔS_tot ≥ 0.
Reversible og irreversible processer
- Reversible proces: En idealiseret proces, hvor systemet hele tiden er i ligevægt, og hvor entropiændringen kun skyldes varmeudveksling (ingen intern produktion af entropi).
- Irreversibel proces: Reelle processer (f.eks. friktion, fri ekspansion, varmeledning) producerer entropi internt — det er derfor, entropien stiger.
Praktiske eksempler
- To legemer med forskellig temperatur, der bringes i kontakt: varme strømmer fra det varmere til det koldere legeme, og den samlede entropi stiger.
- Blanding af to gasser: når gasser blandes spontant, øges antallet af tilgængelige mikrotilstande, og entropien stiger.
- Drevne maskiner og varmemotorer: anden lov sætter en øvre grænse for effektiviteten (Carnotsætningen) — man kan ikke omdanne al varme til arbejde.
Lokale entropifald og totalentropi
Entropi kan falde lokalt (fx når en fryser afkøler indholdet), men det sker kun ved, at entropien andre steder i omgivelserne øges endnu mere. Derfor kan totalentropien for et isoleret system ikke falde.
Begrænsninger og statistisk karakter
Den anden lov er statistisk: for mikroskopiske systemer (få partikler) kan sandsynlige fluktuationer føre til midlertidige, lokale fald i entropi. For makroskopiske systemer med ~10²³ partikler er sådanne fluktuationer praktisk talt umulige at observere, og loven fremstår som deterministisk.
Forbindelse til information
Der er en tæt relation mellem termodynamisk entropi og informationsbegrebet (Shannons entropi). Begge måler usikkerhed eller manglende information om et systems præcise tilstand. Dette forhold bruges aktivt i statistisk fysik og i teorien om termodynamik af beregning (f.eks. Landauers princip).
Sammenfatning
Termodynamikkens anden lov siger i praksis, at energiens og stoffets tendens til at sprede sig fører til en øget entropi i et isoleret system. Udtalelserne af Clausius og Kelvin angiver to ækvivalente måder at formulere denne begrænsning på: varme går spontant fra varmt til koldt, og man kan ikke fuldstændigt omdanne varme til mekanisk arbejde uden tab. Forståelsen af entropi både som et statistisk mål for mikrotilstande og som et termodynamisk mål for energispredning gør anden lov til et centralt koncept i fysik, kemi og ingeniørvidenskab.