Isotoper og forekomst
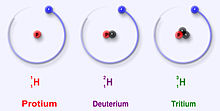
Brint har tre hovedisotoper: protium (1H), deuterium (2H) og tritium (3H). Protium (nucleus = én proton) er langt den mest almindelige form i naturen, deuterium (én proton + én neutron) forekommer i spormængder (ca. 0,015–0,016 % eller omkring 156 ppm af normalt hydrogen), mens tritium (én proton + to neutroner) findes i meget lave mængder og dannes blandt andet ved kosmisk stråling og ved menneskeskabte processer.
Stabilitet og radioaktivitet
Protium og deuterium er stabile isotoper. Tritium er radioaktivt og har en halveringstid på ca. 12,3 år. Tritium udsender beta-stråling med meget lav energi; derfor er ekstern eksponering normalt af begrænset risiko, mens indtag eller indånding kan føre til intern bestråling og bør undgås.
Egenskaber og kemiske forskelle
- Samme elektroniske struktur: Alle brintisotoper har samme antal elektroner og udviser grundlæggende samme kemiske bindingsevner.
- Massens betydning: Forskellen i masse mellem 1H, 2H og 3H giver målbare virkninger på fysiske og kemiske egenskaber. Tyngre isotoper har lavere vibrationsfrekvenser og stærkere bindingskarakter, hvilket fører til såkaldte isotopiske effekter (fx kinetisk isotopeffekt) — reaktioner med deuterium foregår ofte langsommere end med protium.
- Fysiske egenskaber: Forbindelser med deuterium er generelt lidt tungere. Fx er tungt vand (D2O) tættere og har et højere kogepunkt og smeltepunkt end almindeligt vand (H2O) — tæthedsforskellen er i størrelsesordenen ca. 10 %.
- Nukleare egenskaber: Tritium er radioaktivt og bruges ofte som sporstof inden for forskning og industri; det kan også indgå i nuklearfysik og fusionsforsøg.
Anvendelser
- Deuterium: Bruges som tracer i kemiske og biologiske studier, i deutererede opløsningsmidler til NMR-spektroskopi, og i tungt vand (D2O), som fungerer som moderator i visse typer atomreaktorer (fx CANDU-reaktorer).
- Tritium: Anvendes som radiomærkningsstof i forskning, i selvlysende malinger og nødskilte (lave niveauer i små lyskilder), samt som brændstof i fusionsforskning (D–T-fusion giver høj energiydelse). Det er også et nyttigt sporstof i miljø- og hydrologiske undersøgelser.
- Protium: Den almindelige form af brint bruges selvfølgelig i al almindelig kemi og som brændstof (f.eks. i brændselsceller), men omtales sjældent særskilt, da det er standardformen.
Andre brintisotoper
Ved siden af de tre hovedisotoper har forskere frembragt fire andre isotoper (4H til 7H) i laboratorier ved hjælp af acceleratorer. Disse er ekstremt ustabile og har meget korte levetider, så de findes ikke naturligt i miljøet.
Navne og betegnelse
De vigtigste isotoper af brint er unikke ved, at de har egne navne: protium, deuterium og tritium. Deuterium og tritium forkortes ofte som D og T i stedet for 2H og 3H. Den Internationale Union for Ren og Anvendt Kemi (IUPAC) anbefaler dog i formelle sammenhænge brug af massesymbolet (AX), selvom D og T fortsat er almindeligt anvendt og let genkendelige i praksis.
Sikkerhed og miljø
Tritium udgør en særlig sikkerhedsbekymring pga. sin radioaktivitet; det er dog en svag beta-emitter, så den største risiko opstår ved intern eksponering. Tunge mængder af tungt vand (D2O) kan påvirke biologiske processer, men dette kræver at en stor del af kroppens vand erstattes med D2O — noget, der i praksis ikke sker ved normal brug.
Samlet set er brintisotoperne vigtige både i grundforskning og i en række tekniske anvendelser på grund af deres forskellige nukleare og masseafhængige egenskaber.